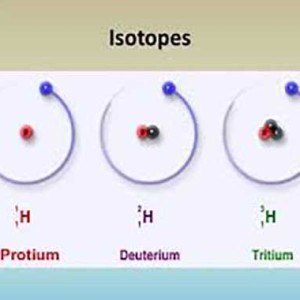
اینجا میخوایم تاریخچه ایزوتوپ را ببینیم
ایزوتوپ به عنصر شیمیایی میگویند که در هسته اتم خود، تعداد پروتون یکسان و تعداد نوترون متفاوت داشته باشد. به عبارت دیگر، ایزوتوپها به عناصری میگویند که تنها در تعداد نوترون با یکدیگر متفاوت باشند. به طور مثال، کربن ۱۲ و ۱۳ و ۱۴، همگی ایزوتوپهای کربن به شمار میآیند. کربن-۱۴ در مجموع ۸ نوترون و کربن-۱۳ در مجموع ۷ نوترون دارند. برای کربن-۱۲ نیز تعداد ۶ نوترون در هسته اتم آن ذکر شده است.
نحوه نمایش ایزوتوپ ایزوتوپها را به طور کلی بوسیله دو روش نشان میدهند: روش اول: نوشتن به صورت «نام عنصر-عدد جرمی ایزوتوپ». به طور مثال، ایزوتوپ اورانیوم به صورت اورانیوم-۲۳۵ و اورانیوم-۲۳۹ نوشته میشود. البته این نوع نوشتار بیشتر در زبان انگلیسی کاربرد دارد و در زبان فارسی، نوشتن خط تیره مرسوم نیست اما بهتر است شکل استاندارد در نوشتن رعایت شود. روش دوم: نوشتن به صورت AZE که در آن، A عدد جرمی، Z عدد اتمی و E نماد عنصر است. به طور مثال، اورانیوم-۲۳۵ را به صورت 235 92 U نشان میدهند. البته از آنجایی که «Z» به طور معمول به کمک نام عنصر مشخص میشود میتوان از نمایش آن صرفنظر کرد. به عنوان نمونه، کربن-۱۴ را به شکل 14 C نشان میدهند.
تعیین تعداد نوترون در یک ایزوتوپ تعداد کل نوترونهای یک ایزوتوپ را میتوان با کم کردن عدد اتمی عنصر از عدد جرمی آن مشخص کرد. به طور مثال، عدد جرمی کربن-۱۲ برابر با ۱۲ و عدد اتمی کربن نیز برابر با ۶ است، بنابراین، تعداد کل نوترونها در کربن-۱۲ برابر با ۶ خواهد بود.
تشکیل ایزوتوپ ایزوتوپها میتوانند به صورت طبیعی و از طریق واپاشی پرتوزای هسته یا به صورت مصنوعی از طریق بمباران هستههای پایدار توسط ذرات باردار به تولید برسند. این بمباران از طریق شتابدهندهها یا نوترون در یک راکتور هستهای انجام میشود. درصد فراوانی ایزوتوپ ایزوتوپهای یک عنصر، همگی با نسبتهای یکسان وجود ندارند. به طور مثال، جیوه دارای هفت ایزوتوپ طبیعی است و هرکدام، درصد فراوانی متفاوتی از 0/146 تا ۲۹/80 درصد دارند. برخی از ایزوتوپهای طبیعی و مصنوعی، ایزوتوپهایی رادیواکتیو هستند. همچنین، تمامی اتمهای سنگینتر از بیسموت، پرتوزا هستند. با این وجود، برخی از نوکلیدهای سبکتر نیز خاصیت رادیواکتیو دارند. به طور مثال، هیدروژن دارای دو ایزوتوپ پایدار اما ایزوتوپ سوم آن یعنی تریتیوم، پرتوزا است.
اندازه گیری درصد فراوانی ایزوتوپ با وجود اینکه نمیتوان به طور مستقیم جرم یک اتم را اندازهگیری کرد، میتوانیم از طیفسنج جرمی بهره بگیریم که اندازهگیری نسبت جرم به بار را ممکن میسازد. در تصویر زیر، ورود گاز کلر به درون دستگاه اسپکترومتر نشان داده شده است. گاز کلر شامل چند ایزوتوپ است و این گاز توسط الکترونها بمباران و یونیزه میشود. یونش و جدایش الکترونها سبب تشکیل یونهای کلر خواهد شد. این یونها پس از شتابدهی، وارد یک میدان مغناطیسی میشوند و این میدان، سبب انحراف جهت حرکت یونها خواهد شد.
اگر پسندیدی، لایک کن و به سازنده انرژی بده!

آفرین عالی بود .
ممنون
زیبا بود👍
ممنون.