10 اسلاید پست توسط: Dispatch انتشار: 4 ساعت پیش 3 مرتبه انجام شده گزارش ذخیره در مورد علاقه ها افزودن به لیست
جدول مندلیف چیست

تاریخچه پیدایش جدول مندلیف
اولین عنصر کشف شده فسفر است. بعد از کشف عناصر، اولین فردی که به دسته بندی عناصر پرداخت، لاوازیه بود. این دانشمند بزرگ، عناصر را به چهار دسته گازها، فلزات، غیرفلزات و عناصر زمین دسته بندی کرد. بعد از او دانشمندان دیگری نیز طبقه بندی های گوناگونی را انجام داند تا سرانجام دمیتری مندلیف توانست با توجه به شباهت های عناصر، آن ها را دسته بندی کند.

جدول طبقه بندی شده مندلیف، بر اساس افزایش جرم اتمی عناصر بوده و در سال 1869 ارائه شد. در این دسته بندی، عناصری که در یک دسته قرار داشتند، دارای خواص مشابهی بودند. عناصر با خواص شیمیای یکسان در یک ستون و عناصر با افزایش جرم اتمی مرتب، در یک دوره قرار گرفتند.

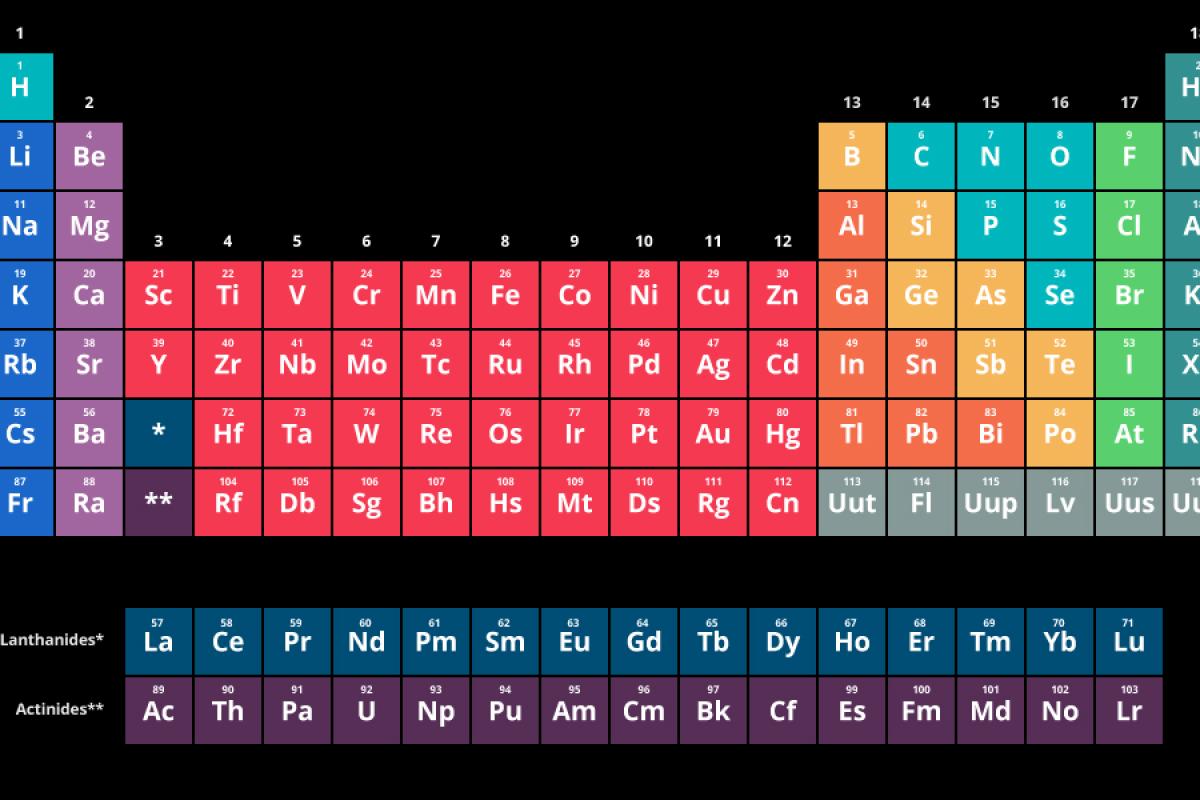
شکل امروزی جدول مندلیف
بین جدول تناوبی امروزی با جدولی که توسط مندلیف ارائه شد تفاوت هایی وجود دارد، ولی اساس کار در هر دو جدول یکی است. اما شگفتی که در جدول ارائه شد، وجود جاهای خالی برای عناصری بود که هنوز کشف نشده بودند. یکی از این عناصر، گالیم بود که مندلیف آن را آکا- آلومینیوم نامگذاری کرده بود. سرانجام با کشف عناصر مختلف، جدول تناوبی به شکل امروزی درآمد. با پیشرفت علم و کشف ذراتی چون الکترون، پروتون و نوترون، جدول مندلیف کامل شد.

جدول مندلیف از 18 گروه یا ستون تشکیل شده است که 8 گروه آن، اصلی و 10 گروه آن، فلزات واسطه هستند. فلزات واسطه گروه های 3 تا 12 جدول تناوبی را تشکیل می دهند. اما هشت گروه اصلی شامل گروه اول اصلی (فلزات قلیایی)، گروه دوم اصلی (فلزات قلیایی خاکی)، گروه های سوم تا ششم اصلی، گروه هفتم اصلی (هالوژن ها) و گروه هشتم اصلی (گازهای نجیب) هستند.
امروزه تمام 118 عنصر جدول مندلیف شناسایی و در خانه های خود قرار داده شده و نام گذاری شدند. هر عنصر با نماد شیمیایی مخصوص خود نوشته شده و عدد اتمی (تعداد پروتون های اتم) و عدد جرمی (مجموع تعداد پروتون ها و نوترون های اتم) در کنار این نماد نوشته می شود.

عناصر گروه اول اصلی یا فلزات قلیایی
این گروه از عناصر شامل لیتیم، سدیم، پتاسیم، روبیدیوم، سزیم و فرانسیم است. در لایه ظرفیت این عناصر، فقط یک الکترون وجود دارد به همین دلیل میل به واکنش پذیری بالایی دارند. با از دست دادن یک الکترون لایه ی والانس، به آرایش پایدار گاز نجیب می رسند. به دلیل خاصیت واکنش پذیری بالا، این عناصر را در ترکیبات روغنی مانند نفت نگهداری می کنند تا اکسید نشوند. سطح فلزات قلیایی براق و صیقلی بوده و به جهت نرم بودن، به راحتی با چاقو برش داده می شوند. در اثر واکنش با آب، محلول قلیایی تولید می کنند. از این واکنش، گاز هیدروژن آزاد می شود.

گروه هفتم اصلی یا هالوژن ها
گروه 17 از جدول تناوبی که به گروه 7 اصلی و هالوژن ها نیز معروف است، شامل فلوئور، کلر، برم، ید و استاتین است. در لایه والانس این عناصر، 7 الکترون وجود دارد، پس تمایل به گرفتن یک الکترون و رسیدن به آرایش پایدار هشتایی را دارند. در این حالت، عناصر منجر به تشکیل آنیون هایی با یک بار منفی مانند کلرید (Cl-) می شوند. فلوئور و کلر به شکل گاز، برم به شکل مایع و ید در حالت طبیعی جامد است.
کاربرد اصلی قرص برای ضدعفونی کردن آب استخر است. این ماده به سه شکل قرص کلر، پودر کلر و کلر مایع مورد استفاده قرار می گیرد.
هالوژن از جمله مواد سمی بوده و تولید آن از نمک و مواد معدنی است. اگر این مواد با هیدروژن ترکیب شود، تولید اسید می کنند. رفتارهایی که از این عناصر سر می زند، روند تناوبی دارد، به جزء فلوئور که دارای رفتارهای متفاوت و استثنایی است.

گروه هشتم اصلی یا گازهای نجیب
از مهمترین ویژگی های گازهای نجیب، تمایل نداشتن به واکنش پذیری و بی اثر بودن آن هاست. همه این عناصر به شکل گاز بوده و به شکل تک اتمی در طبیعت وجود دارند. رنگ و بویی در این گازها دیده نشده و به گروه 18 از جدول مندلیف تعلق دارند.

گروه هشتم اصلی یا گازهای نجیب
از مهمترین ویژگی های گازهای نجیب، تمایل نداشتن به واکنش پذیری و بی اثر بودن آن هاست. همه این عناصر به شکل گاز بوده و به شکل تک اتمی در طبیعت وجود دارند. رنگ و بویی در این گازها دیده نشده و به گروه 18 از جدول مندلیف تعلق دارند.

فلزات واسطه
عناصر فلزات واسطه از گروه های 3 تا 12 جدول تناوبی را شامل شده و اوربیتال d آن ها در حال پر شدن از الکترون است. به این فلزات، فلزات واسطه خارجی می گویند. دو دسته از عناصر به نام لانتانیدها و اکتنیدها که اوربیتال f آن ها در حال پرشدن است، نیز در دسته عناصر فلزات واسطه قرار گرفته و به نام فلزات واسطه داخلی خوانده می شوند.
فلزات واسطه خارجی، چون دارای انتقال الکترونی بین اوربیتال های d هستند، تشکیل ترکیبات رنگی می دهند. ترکیبات این فلزات دارای اعداد اکسایش متفاوت بوده و می توانند ترکیبات پارامغناطیسی تشکیل دهند. این فلزات سخت بوده و میل به واکنش پذیری کمتری نسبت به فلزات قلیایی خاکی دارند.

تشکیل ترکیبات مختلفی چون کربومر
از اتصال اتم های عناصر مختلف به هم، ترکیبات شیمیایی تشکیل می شوند. مواد مختلف در نتیجه وجود ترکیبات متفاوت به وجود می آیند. یکی از این ترکیبات به نام کربومر است. کربومر به پلیمری از اسیداکریلیک گفته می شود که وزن مولکولی بالایی داشته و مصنوعی است. کربومر در حضور آب، با از دست دادن پروتون های خود، به آنیون تبدیل می شود. به دلیل داشتن این ویژگی، می تواند آب را تا چندین برابر حجم خود جذب کرده و یک پلی الکترولیت باشد. کاربرد اصلی کربومر در محصولات آرایشی برای کنترل ویسکوزیته آن هاست. بنابراین در ترکیب ژل های مرطوب کننده پوست، شامپو، ضد آفتاب، کرم چشم و ... مورد استفاده قرار می گیرند.
10 اسلاید
1
نتیجه
مجموع امتیاز شما
امتیاز
تعداد پاسخ صحیح
تعداد پاسخ غلط
درصد صحیح
شما به درصد سوالات پاسخ درست دادید
اگر پسندیدی، لایک کن و به سازنده انرژی بده!
8 لایک


فرصتت جایزه بده پلیز