16 اسلاید پست توسط: آریان خبیث انتشار: 2 ماه پیش 8 مرتبه انجام شده گزارش ذخیره در مورد علاقه ها افزودن به لیست
های باحالا چطورید با یه پست فوق العاده مفید که بدردتون میخوره آوردم
در علم شیمی به مادهای خالص گفته میشود که اتمهای سازنده آن از تعداد پروتونهای برابری در هستهٔ خود برخوردار باشند. این عدد (تعداد پروتونها) که با نماد Z نشان داده میشود، عدد اتمی آن عنصر نام دارد. همهٔ اتمهایی که دارای تعداد پروتونهای برابر (عدد اتمی برابر) باشند، ویژگیهای شیمیایی یکسانی دارند. اما اتمهای یک عنصر میتوانند دارای تعداد متفاوتی (نوترون) باشند که (ایزوتوپ)های آن عنصر نامیده میشوند. گاهی نیز برای سادگی، به عنصر شیمیایی صرفاً عنصر گفته میشود. ویژگیهای شیمیایی اتمهای یک عنصر که توسط ساختار الکترونی آنها تعیین میشود که آن نیز به تعداد پروتونهای هسته آن اتم وابسته است. در بیان کلی مفهوم عنصر به ویژگی یک اتم گفته میشود که آن را از سایر ویژگیهایی که اتمهای دیگر دارند متمایز میکند. منظور از ویژگی در حالت کلی به تعداد پروتونهای یک اتم در هستهٔ خود گفته میشود که ویژگی آن را شکل میدهد این همان ویژگی است که بهطور مثال اتم مس را از طلا متمایز میکند. تمام عناصر شیمیایی از باریون ساخته شدهاند. با این وجود کیهان شناسان بر این باورند که باریون تنها ۱۵٪ مواد قابل مشاهده در کیهان را تشکیل میدهند؛ بنابراین باقیماندهٔ مواد موجود در کیهان، مادهٔ تاریک است که ماهیت آن شناخته شده نیست ولی از عناصری که ما میشناسیم تشکیل نشدهاست. از بین تمام عناصر دو عنصر هیدروژن و هلیم که در بدو مه بانگ (بیگ بنگ) تشکیل شدهاند، فراوانترین عناصر موجود در کائنات هستند.

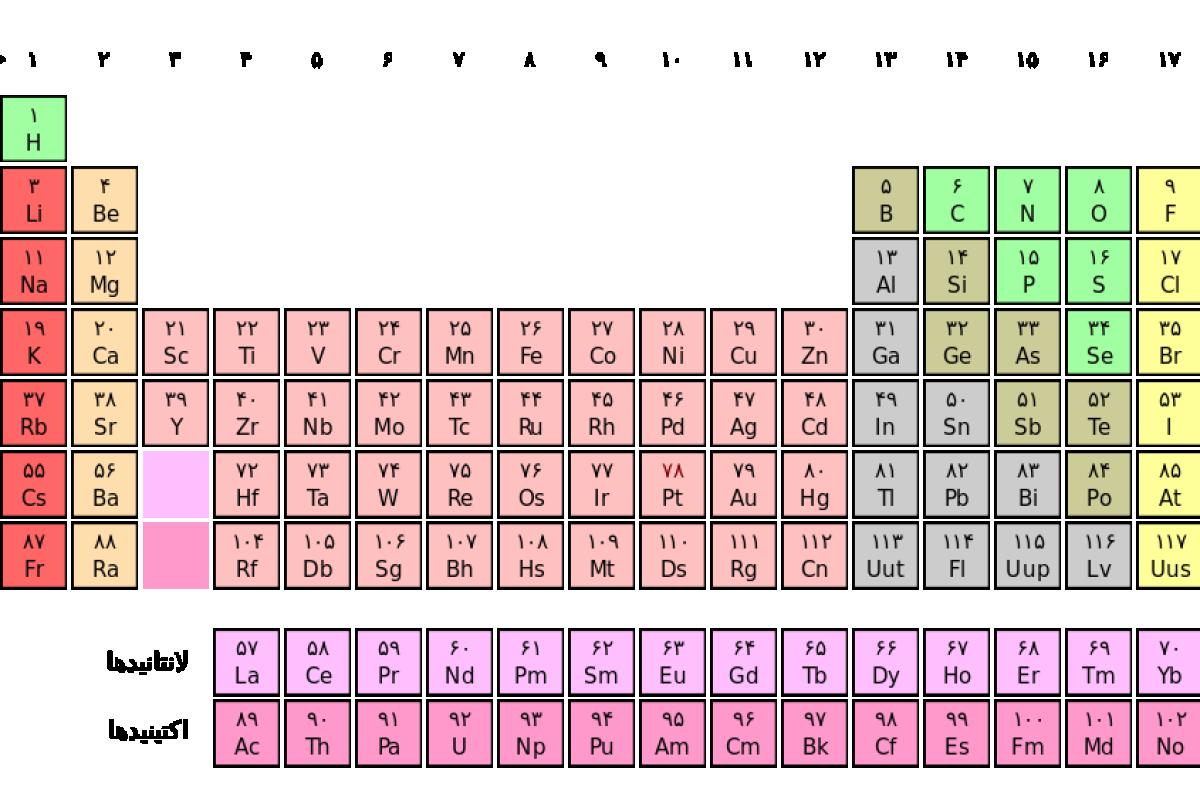
جدول تناوبی عناصر پیش از سال ۱۳۹۵ با توجه به عناصر ۱۱۳ تا ۱۱۸ که نامهایشان به تازگی تغییر کردهاست. به ترتیب از ۱۱۳ به بعد: نیونیم_فلوریم_مسکوویم_لیورموریم_ودر آخر اوگانسون
عناصر شیمیایی میتوانند در هنگام واکنش شیمیایی با یکدیگر ترکیب شده و تعداد بیشماری مادهٔ شیمیایی بهوجود آورند؛ مثلاً آب نتیجهٔ واکنش عنصرهای هیدروژن و اکسیژن است. در این حالت، دو اتم هیدروژن و یک اتم اکسیژن به هم متصل میشوند و مولکولی با فرمول شیمیایی H2O میسازند. همین دو عنصر در شرایط متفاوت میتوانند مادهٔ دیگری را به نام هیدروژن پراکسید (آب اکسیژنه) بسازند که دارای مولکولهای H2O2 است. به همین شکل، همه ترکیبهای شیمیایی میتوانند به عناصر سازنده خود تجزیه شوند. به عنوان مثال میتوان آب را به کمک برقکافت به عناصر هیدروژن و اکسیژن تبدیل کرد.
یک مادهٔ خالص که تنها از اتمهای یک عنصر تشکیل شده باشد، «مادهٔ ساده» نامیده میشود. چنین مادهای را نمیتوان به ماده دیگری تجزیه کرد. از این دیدگاه، مادهٔ ساده در برابر مادهٔ مرکب قرار میگیرد. به عنوان مثال، اکسیژن یک عنصر است. اما مادهای را که ما در طبیعت به عنوان گاز اکسیژن شناختهایم، در حقیقت یک ماده ساده دو اتمی از این عنصر است که «دی اکسیژن» یا «اکسیژن مولکولی» (O2) نامیده میشود. اوزون شکل دیگری از عنصر اکسیژن است که در طبیعت با فرمول (O3) یافت میشود. رابطه بین دی اکسیژن و اوزون رابطهای است که به آن دگرشکلی (آلوتروپی) میگویند. به زبان دیگر، دی اکسیژن و اوزون، دگرشکلهای عنصر اکسیژن هستند. الماس و گرافیت نیز دو آلوتروپ برای عنصر کربن هستند. عناصر دیگر مانند گوگرد و فسفر هم دارای آلوتروپهای شناختهشدهٔ پرکاربردی هستند. از بین عناصر شناخته شده تعداد کمی به صورت ساده یا خالص در طبیعت یافت میشوند که از بین آنها میتوان به مس، طلا، نقره، کربن و گوگرد اشاره کرد. به جز چند عنصر بقیه عناصر از جمله گازهای نجیب (گازهای بی اثر) و فلزات نجیب معمولاً به صورت ترکیب یافته بر روی زمین کشف میشوند و نه به صورت خالص.
عناصر شیمیایی را نمیتوان به کمک واکنشهای شیمیایی معمولی به یکدیگر تبدیل کرد. تنها واکنشی که میتوان با استفاده از آن تعداد پروتونهای هسته اتمهای یک عنصر را تغییر داد و یک عنصر را به عنصر دیگری تبدیل کرد، یک واکنش هستهای است که آن را واکنش تبدیل هستهای مینامند.
پیش از سال ۲۰۱۶ تعداد ۱۱۸ عنصر، کشف یا ساخته شدهبود. از این تعداد، ۹۲ عنصر در طبیعت یافت میشدند و بقیه بهطور مصنوعی و به کمک واکنشهای هستهای در آزمایشگاه ساخته شدهاند. از میان همه عناصر، ۸۱ عنصر دارای حداقل یک ایزوتوپ پایدار میباشند که به جز عنصر شماره ۴۳ (تکنسیم) و عنصر شماره ۶۱ (پرومتیم) همگی دارای عدد اتمی برابر یا پایینتر از ۸۳ هستند. به زبان دیگر در جدول تناوبی تنها عناصری که از عنصر ۸۴ (پولونیوم) سبکتر بوده و دارای ایزوتوپ پایدار نمیباشند، تکنسیم و پرومتیم هستند. به جز ۸۱ عنصر مذکور بقیه ایزوتوپ پرتوزا (رادیو نوکلئید) بوده که در طول زمان و در پی واپاشی هستهای به عناصر دیگر تبدیل میشوند.
تا نوامبر ۲۰۱۶، بنا بر گزارش اتحادیه بینالمللی شیمی محض و کاربردی در مجموع ۱۱۸ عنصر را شناسایی کرده بود. اولین ۹۴ عنصر بهطور طبیعی روی زمین یافت میشوند و ۲۴ باقیمانده عناصر مصنوعی هستند که در واکنشهای هستهای تولید میشوند. به جز عناصر رادیواکتیو ناپایدار (رادیونوکلئیدها) که به سرعت تجزیه میشوند، تقریباً همه عناصر به صورت صنعتی در مقادیر مختلف در دسترس هستند. کشف و سنتز عناصر جدید بیشتر حوزهای است که بهطور مداوم مورد مطالعه علمی قرار دارد.
عدد اتمی
عدد اتمی یک عنصر که با Z نشان داده میشود، برابر با تعداد پروتونهایی است که در هسته اتمهای آن عنصر یافت میشود. برای مثال، تمام اتمهای هیدروژن تنها یک پروتون در هسته خود دارند. به همین دلیل، عدد اتمی هیدروژن برابر با یک است. اما ممکن است که هسته اتمهای یک عنصر، دارای تعداد نوترونهای متفاوت باشند، که هر کدام نشانگر ایزوتوپهای متفاوت آن عنصر هستند.
اتمهای یک عنصر از دیدگاه الکتریکی خنثی هستند؛ زیرا تعداد الکترونهای آن که دارای بار منفی هستند با تعداد پروتونهای آن که دارای بار مثبت هستند برابر است. به همین دلیل، عدد اتمی اتمهای یک عنصر هم نشان دهنده تعداد پروتونها و هم الکترونهای آن است. ویژگیهای شیمیایی یک عنصر بیش از هر چیز با آرایش الکترونی آن تعیین میشود. میتوان گفت که شناخت عدد اتمی یک عنصر به شناخت ماهیت آن عنصر کمک میکند. عدد اتمی یک عنصر را در گوشه سمت چپ و پایین نماد آن عنصر به صورت zX مینویسند.
گاهی اصطلاح سبک یا سنگین به صورت غیررسمی برای اشاره به عدد اتمی نسبی عنصر (و نه چگالی آن) استفاده میشود؛ مثلاً عناصر سبکتر از کربن یا عناصر سنگینتر از سرب. هر چند وزن یا جرم اتمهای یک عنصر همانند عدد اتمی آن از یک روند افزایشی با آهنگ ثابت برخوردار نیست.
عدد جرمی
ویرایش
عدد جرمی یک عنصر که با A نشان داده میشود، برابر است با مجموع تعداد نوکلئونها (پروتون و نوترون) در داخل هسته اتمهای آن عنصر. عدد جرمی معمولاً در کنار نماد عنصر نشان داده نمیشود؛ مگر این که بخواهیم به تفاوت ایزوتوپهای آن عنصر اشاره کنیم. برای نشان دادن عدد جرمی در کنار نماد شیمیایی عنصر، باید آن را در گوشه سمت چپ و بالای آن به صورت AX نوشت.
اگرچه تعداد پروتونهای اتمهای یک عنصر همواره برابر است؛ ولی اتمهای یک عنصر میتوانند دارای تعداد نوترونهای متفاوت و در نتیجه عدد جرمی متفاوت (ایزوتوپهای متفاوت) باشند. برای مثال، هیدروژن دارای سه ایزوتوپ اصلی است که عبارتند از:
●پروتیوم یا هیدروژن معمولی که هسته آن فاقد نوترون است و با نماد H نمایش داده میشود،
●دوتریوم کمیابتر بوده و هسته آن دارای یک نوترون و یک پروتون است (گاهی با نماد 2H و بعضی مواقع با نماد D نشان داده میشود)
●و تریتیم که هیدروژن پرتوزا است و در طبیعت به تعداد بسیار کم یافت شده و در هسته خود دارای دو نوترون و یک پروتون است (میتوان این ایزوتوپ را با نماد 3H یا T هم نشان داد).
تغییر عدد جرمی تأثیری بر روی آرایش الکترونی اتمهای یک عنصر ندارد؛ پس انتظار داریم ایزوتوپهای یک عنصر خواص شیمیایی یکسانی داشته باشند که معمولاً همینطور است؛ اما اثرات ایزوتوپیک (تغییرات عدد جرمی) میتوانند در اتمهای سبک (لیتیم، هیدروژن و هلیم) به راحتی مشاهده شوند؛ زیرا اضافه یا کم شدن یک نوترون در هسته این اتمها منجر به تغییرات نسبتاً مشهود در جرم اتم میشود که بر روی سینتیک واکنشهای شیمیایی و استواری پیوندهای شیمیایی تأثیرگذار است. عدد جرمی، برای ۱۱۵ عنصر دیگر، اثر چندانی بر روی خواص شیمیایی عنصر ندارد.
جرم اتمی
جرم اتمی هر اتم، عددی است حقیقی که برابر است با جرم هر ایزوتوپ خاص از اتم یک عنصر که با واحد یکای جرم اتمی (U) نشان داده میشود. به دلیل برابر واحد U نبودن جرم پروتون و نوترون، بیشتر بودن تعداد نوترونها از پروتونها و ناچیز بودن جرم الکترونها و همچنین به خاطر وجود انرژی بستگی هستهای، عدد جرمی با جرم اتمی متفاوت است. به عنوان مثال، جرم اتمی کلر-۳۵ تا پنج رقم معنیدار برابر با ۳۴/۹۶۹U و وزن اتمی کلر-۳۷ برابر با ۳۶/۹۶۶U میباشد. جرم اتمی یک ایزوتوپ خالص یک عنصر بر حسب U بسیار به عدد جرمی آن نزدیک میباشد. تنها استثنا در مورد جرم اتمی ایزوتوپی از یک عنصر که از لحاظ ریاضی یک عدد حقیقی نیست، ایزوتوپ کربن-۱۲ است که مقدار آن بر حسب تعریف، دقیقاً برابر با دوازده U میباشد؛ زیرا یکای جرم اتمی به صورت یک دوازدهم جرم ایزوتوپ آزاد و بدون بار کربن-۱۲ در حالت پایه تعریف میشود. جرم اتمی نسبی یا همان وزن اتمی (اصطلاح مشهور و تاریخی برای جرم اتمی نسبی) هر عنصر در واقع میانگین جرمهای اتمی تمام ایزوتوپهای آن عنصر با توجه به درصد فراوانی آنها است. برای مثال جرم اتمی نسبی کلر برابر با ۳۵/۴۵۳U است که اختلاف معنیداری با عدد طبیعی منظور شده برای کلر (۳۵) دارد. علت آن، وجود دو ایزوتوپ با درصدهای فراوانی متفاوت در طبیعت است: کلر-۳۵ با درصد فراوانی ۷۶٪ و کلر-۳۷ با درصد فراوانی ۲۴٪.
ایزوتوپ
ایزوتوپهای یک عنصر، اتمهایی با تعداد پروتونهای برابر و تعداد نوترونهای متفاوت میباشند. برای مثال، عنصر کربن سه ایزوتوپ اصلی دارد. تمام اتمهای کربن دارای شش پروتون در درون هسته خود هستند؛. ولی میتوانند دارای شش، هفت یا هشت نوترون باشند؛ بنابراین سه ایزوتوپ کربن به ترتیب دارای عدد جرمی ۱۲، ۱۳ و ۱۴ بوده و کربن-۱۲، کربن-۱۳ و کربن-۱۴ نام دارند.
به جز هیدروژن که ایزوتوپهای آن دارای جرم نسبی بسیار متفاوت با یکدیگر و در نتیجه اثرات شیمیایی متفاوت میباشند، ایزوتوپهای دیگر عناصر به راحتی از هم قابل شناسایی نیستند.
تمام عناصر دارای تعدادی ایزوتوپ رادیواکتیو یا رادیوایزوتوپ میباشند. هر چند تمام این رادیوایزوتوپها طبیعی نیستند. رادیوایزوتوپها معمولاً با تابش پرتو آلفا یا پرتو بتا به عناصر دیگری تبدیل میشوند. ایزوتوپهای غیر رادیو اکتیو از هر عنصر، ایزوتوپ پایدار نام دارند. تمام ایزوتوپهای پایدار شناخته شده به صورت طبیعی یافت میشوند. بیشتر عناصری که در طبیعت یافت میشوند، بیش از یک ایزوتوپ پایدار دارند. بسیاری از رادیوایزوتوپها که در طبیعت یافت نمیشوند، پس از سنتز مصنوعی توصیف و معرفی میشوند. برخی عناصر نیز دارای هیچ ایزوتوپ پایداری نیستند که عنصر پایدار نامیده میشوند و به عکس برخی تنها دارای ایزوتوپهای رادیواکتیو میباشند. تمام عناصری که دارای عدد اتمی بیشتر از ۸۲ باشند در این دسته قرار دارند.
دگرشکل
اتمهای عناصر خالص میتوانند با یکدیگر بیش از یک نوع پیوند، ایجاد کرده و در نتیجه با چندین ساختار متفاوت مشاهده شوند. به این اشکال مختلف، آلوتروپ میگویند. آلوتروپها در خواص شیمیایی با یکدیگر متفاوت هستند. برای مثال، کربن میتواند به شکل الماس با ساختار چهاروجهی در اطراف هر اتم کربن، به شکل گرافیت با ساختار لایهلایه و شش وجهی، به شکل گرافین که تشکیل شده از یک لایه گرافیت و بسیار مستحکم است یا به شکل فولرن با ساختار کروی یافت شود. ریزلولههای کربن نیز یکی دیگر از آلوتروپهای کربن هستند که از لولههایی با ساختار شش وجهی تشکیل شدهاند (که حتی در خواص الکتریکی نیز میتوانند با یکدیگر متفاوت باشند). توانایی یک عنصر برای وجود داشتن به اشکال مختلف آلوتروپی نامیده میشود.
حالت استاندارد یک عنصر شیمیایی، شکلی از آن عنصر است که آنتالپی استاندارد تشکیل آن در شرایط طبیعی کمینه باشد. طبق قرارداد، کمترین آنتالپی استاندارد تشکیل را در محاسبات برابر با صفر در نظر میگیرند. برای مثال حالت استاندارد کربن، گرافیت است؛ زیرا پایدارترین آلوتروپ در بین همه ساختارهای کربن میباشد.
خلوص شیمیایی و خلوص ایزوتوپیک
خلوص شیمیایی با خلوص ایزوتوپیک متفاوت است. عنصر خالص ماده ای است که اتمهای آن دارای عدد اتمی یکسان یا تعداد پروتونهای یکسان باشند. در حالیکه از دیدگاه ایزوتوپیک عنصر خالص عنصری است که تنها دارای یک ایزوتوپ پایدار باشد.
برای مثال اگر ۹۹/۹۹٪ اتمهای یک سیم مسی از اتمهای مسی که همگی دارای ۲۹ پروتون باشند، تشکیل شده باشد، از دیدگاه شیمیایی خالص است. اما مس از دیدگاه ایزوتوپیک خالص نیست زیرا مس معمولی از دو ایزوتوپ پایدار
cu
63
{\displaystyle {\ce {^{63}cu}}}به میزان ۶۹٪ و
Cu
65
{\displaystyle {\ce {^{65}Cu}}}به میزان ۳۱٪ با تعداد نوترونهای متفاوت تشکیل شدهاست. برخی عناصر مانند طلای خالص هم از دیدگاه ایزوتوپیک و هم شیمیایی خالص هستند زیرا طلای معمولی تنها دارای یک ایزوتوپ (
Au
197
{\displaystyle {\ce {^{197}Au}}}) میباشد.
16 اسلاید
1
نتیجه
مجموع امتیاز شما
امتیاز
تعداد پاسخ صحیح
تعداد پاسخ غلط
درصد صحیح
شما به درصد سوالات پاسخ درست دادید
اگر پسندیدی، لایک کن و به سازنده انرژی بده!
5 لایک


نظرات بازدیدکنندگان (0)